【皓元·服务】迎战药典0862新规:皓元医药元素杂质研究全服务已就位
2025版《中国药典》即将在今年10月1日正式实施,其中在通则部分重磅新增了0862 元素杂质限度和测定法。这一举措标志着我国对药品元素杂质控制的要求与ICH Q3D等国际标准全面接轨,元素杂质控制已成为药物全生命周期中不可或缺的刚性环节。
为何元素杂质控制如此重要?
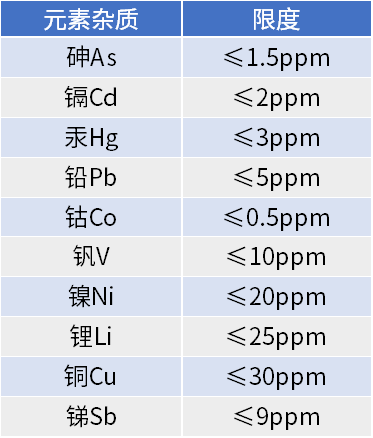
在药物研发与生产过程中,元素杂质可能通过原料、辅料、生产设备、水和包装材料等多种途径引入。这些元素杂质不能为患者提供任何治疗作用,某些元素杂质甚至有一定毒性,例如镉Cd、铅Pb、砷As、汞Hg等,即使含量极低,也可能具有显著的毒性、致癌性或致突变性,潜在威胁患者健康,所以它们在药品中需要被控制在合理的限度范围内。
在药物研发、生产及质量控制中,严格对元素杂质进行识别、评估和控制,是确保药品安全有效、保障患者用药安全的核心前提,也是药品申报注册(IND/NDA/ANDA)中必须提交的关键研究资料。
新通则0862核心内容简述
新增的0862通则主要借鉴了ICH Q3D的理念框架,其核心内容可概括为:
1、分类与风险评估
基于元素杂质的毒性和药品中出现的可能性,参考ICH Q3D,将元素杂质分为3类,1类(人类毒素,在药品生产中应限制使用或禁止)、2类(给药途经依赖型的人体毒素,又分为2A和2B)和3类(口服途径毒性相对较低,但吸入和注射给药途经仍需考虑);并规定了不同给药途径(口服、注射、吸入等)的每日允许暴露量(PDE)。
2、控制策略
要求药品生产企业基于风险评估,对药品生产全过程可能引入的元素杂质来源进行系统分析,并制定相应的控制策略。这意味着不能仅依赖终产品检测,更需要从源头和过程进行管控。
3、检测方法
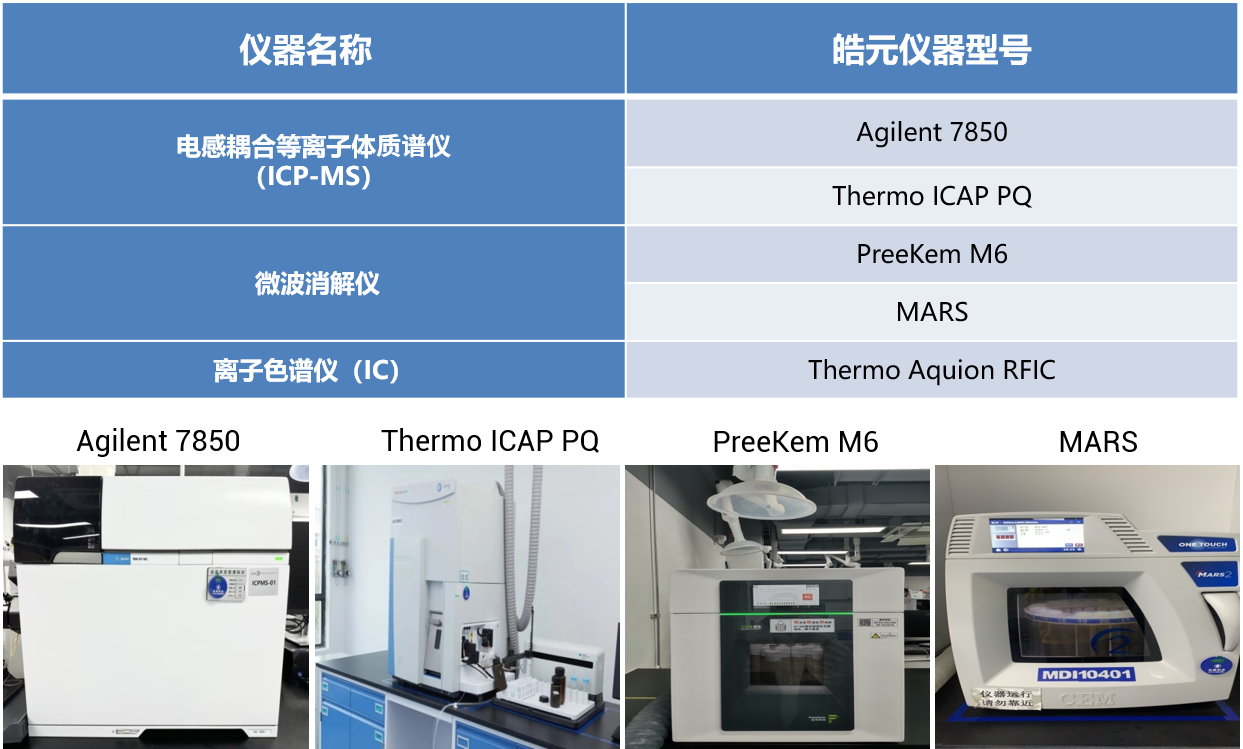
明确推荐使用电感耦合等离子体质谱法(ICP-MS)、电感耦合等离子体原子发射光谱法(ICP-OES)、原子吸收分光光度法(AAS)、X射线荧光光谱法、重金属检查等其他合适的技术手段。其中ICP-MS 作为高灵敏度、多元素同时分析的优选方法。
4、确认与验证
以上推荐的各种方法均需要经过分析方法验证,以证明分析方法满足预期的质量控制的目的。对分析方法的专属性、准确度、精密度、检测限/定量限、线性和范围、耐用性等提出了明确的验证要求,以确保检测结果的科学、准确和可靠。
应对新规挑战?皓元医药分析服务平台元素杂质一站式解决方案为您护航!
新规的出台无疑对药企的分析检测能力提出了极高要求。建立符合药典要求的ICP-MS方法并进行完整的方法学验证,需要专业的技术团队、顶尖的仪器平台和丰富的项目经验。上海皓元医药股份有限公司分析服务平台依托顶尖的分析仪器设备和资深的专家团队,为您提供一站式的元素杂质研究解决方案,助力您轻松应对新规。
我们的服务

我们的优势

案例分享
皓元医药分析服务平台采用有机溶剂NMP溶解后直接上机检测,成功开发出了更高效、准确、可靠的ICP-MS检测分析方法。前处理时间大大缩短,且减少了可能的污染来源途径。
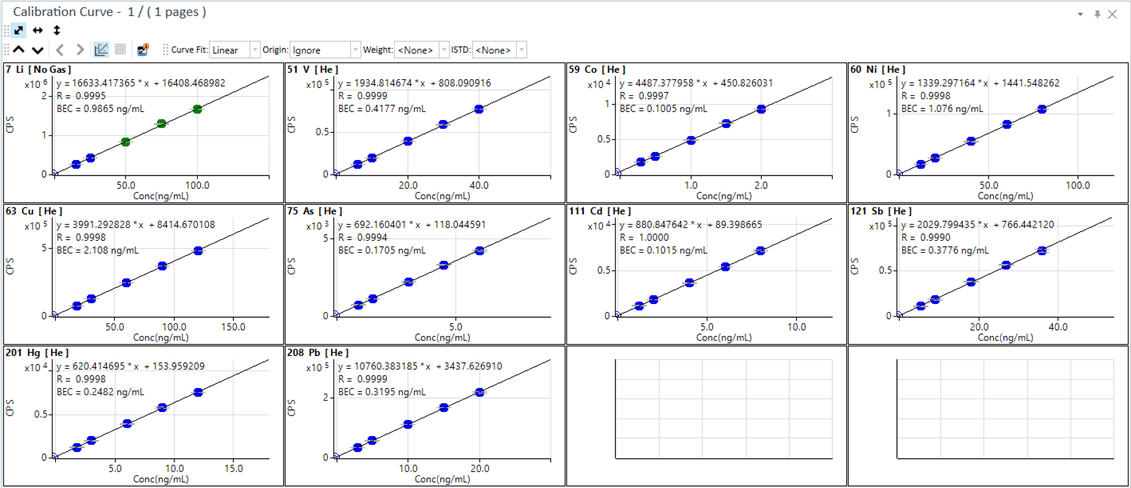
△10个元素线性结果图
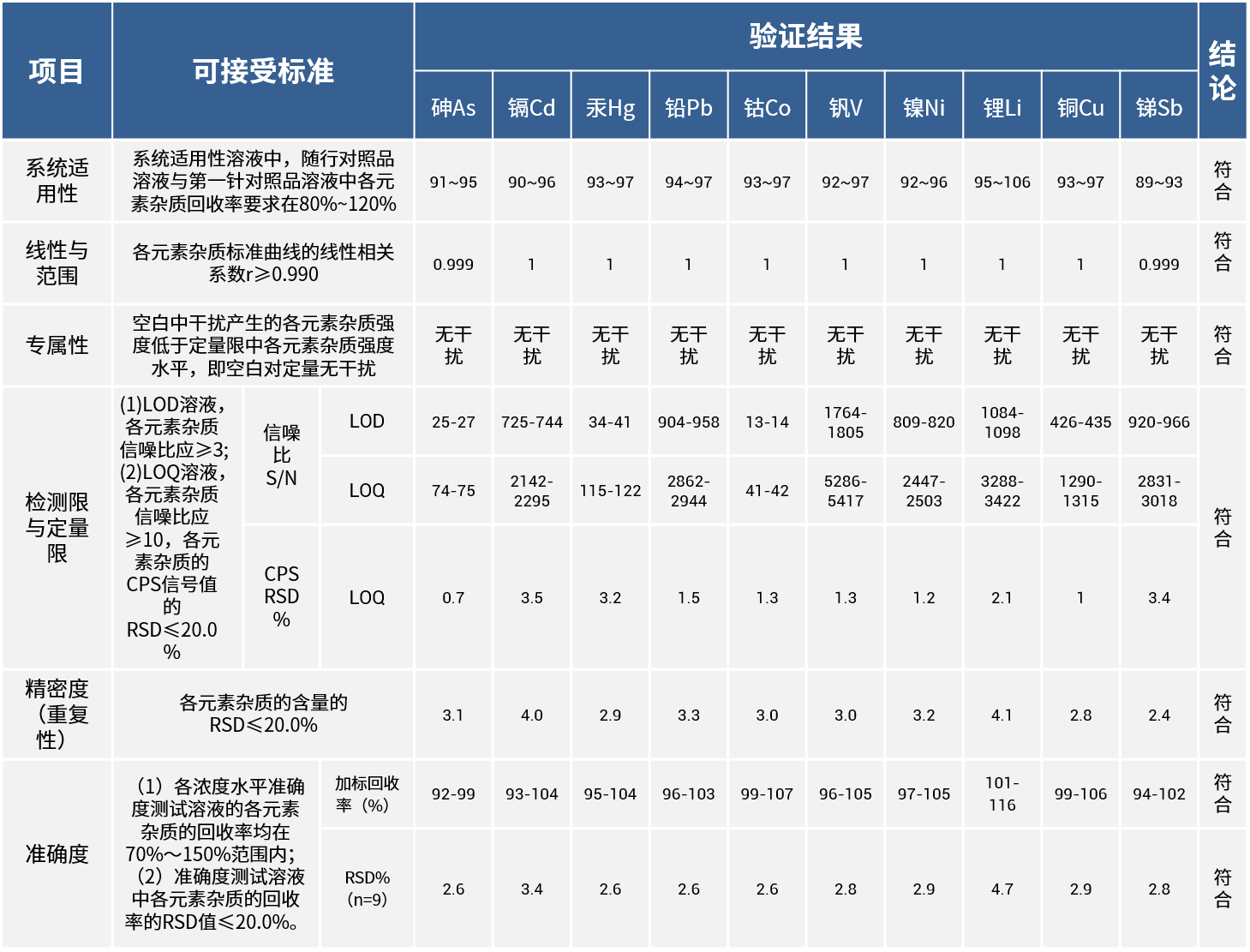
△方法验证结果表
上海皓元医药股份有限公司
Phone: 15000728212 (张经理)
Tel: 021-6163 0697 转 6215
Web: www.chemexpress.com
Email: zl3448@chemexpress.com.cn /ASU-services@chemexpress.com.cn
Address: 上海市浦东新区张衡路1999弄3号楼

