多肽偶联药物 (PDC) 开发
PDC凭借其小分子量、高穿透力、以及高效的合成工艺,正在成为继ADC后,肿瘤靶向治疗领域的革命性创新。预计到2030年,全球PDC市场规模将突破128.43亿美元,年均增长率预计为19.2%。
皓元医药依托深厚的多肽研发能力与先进的载荷-连接子平台,为PDC药物开发提供全链条技术赋能。与皓元医药合作,加速您的PDC药物管道开发,助力PDC药物商业化进程!
来源: Grand view Research: Peptide Drug Conjugates Market Size, Industry Report, 2030

一站式PDC CDMO服务
皓元医药提供从载荷-连接子、多肽合成和偶联到PDC原液和制剂的全方位服务,实现高效的规模化生产和无缝的技术转移

丰富的项目经验与丰富库存
皓元医药具备80+ 库存载荷、400+ 库存连接子,以及 1,000+ 连接子合成经验和1,500+ 多肽合成经验,助力完成300+ PDC化合物开发

质量合规
研发符合 ISO9001 体系,生产遵循 GMP 标准,满足中国、美国及欧盟的法规要求,为您的PDC药物开发提供质量保障
我们的服务
皓元医药提供从PDC研发到商业化生产的全流程服务,支持您的 PDC 项目在各个阶段的需求。立即联系我们,共同推进更快速、更可靠、更安全的 PDC 药物开发。
我们的服务项目包括
多肽高通量合成
- 36/48多通道多肽合成仪,同时合成48种不同序列的多肽
- 合成规模:每个通道0.05-0.1 mmol (1-10mg)
- 序列长度:3-60AA
- 自动纯化收集
- 快速交付:20-30 个常规氨基酸,平均 2 周交付
多肽定制合成
- 固相合成及液相合成
- 氮端修饰:Acetyl, Carbamate, PEGylation, Biotinylation、荧光标记、DOTA等螯合剂等
- 环肽:TATA 成环、1对二硫键、2对二硫键、3对二硫键、click环、酰胺环、click和二硫键双环、订书肽等
- C端修饰:Camides, Esters, AMC
- GLP-1类衍生物
多肽质量控制
- 杂质研究
- 手型杂质分析
- MS/MS- 测序、N- 测序、核磁、氨基酸组成、对应异构体、含量、溶剂残留、重金属、微生物、内毒素等
载荷-连接子合成&分析
- 微管抑制剂:MMAE, MMAD, MMAF, DM1, DM4
- 靶向DNA药物负载物:PBD
- 酶抑制剂:Dxd, SN38, Exatecan
- 可裂解连接子/不可裂解连接子
- 工艺参数优化
- 不稳定中间体稳定性研究
- 纯化方法研究
- 基因毒杂质研究
- 工艺表征及验证
开发&生产
PDC 原液开发
- 偶联工艺开发及验证
- 放大工艺开发
PDC 制剂开发
- 处方前研究
- 预稳定性试验
- 处方筛选
- 辅料及包材的相容性研究
- 冻干工艺开发和优化
- 2ml, 20ml, 50ml等全规格水针和冻干生产线
PDC 分析
- 结构表征
- 质量放行
- 稳定性研究
- IND/ NDA申报
合作优势
我们的基地
研发及生产基地
案例研究
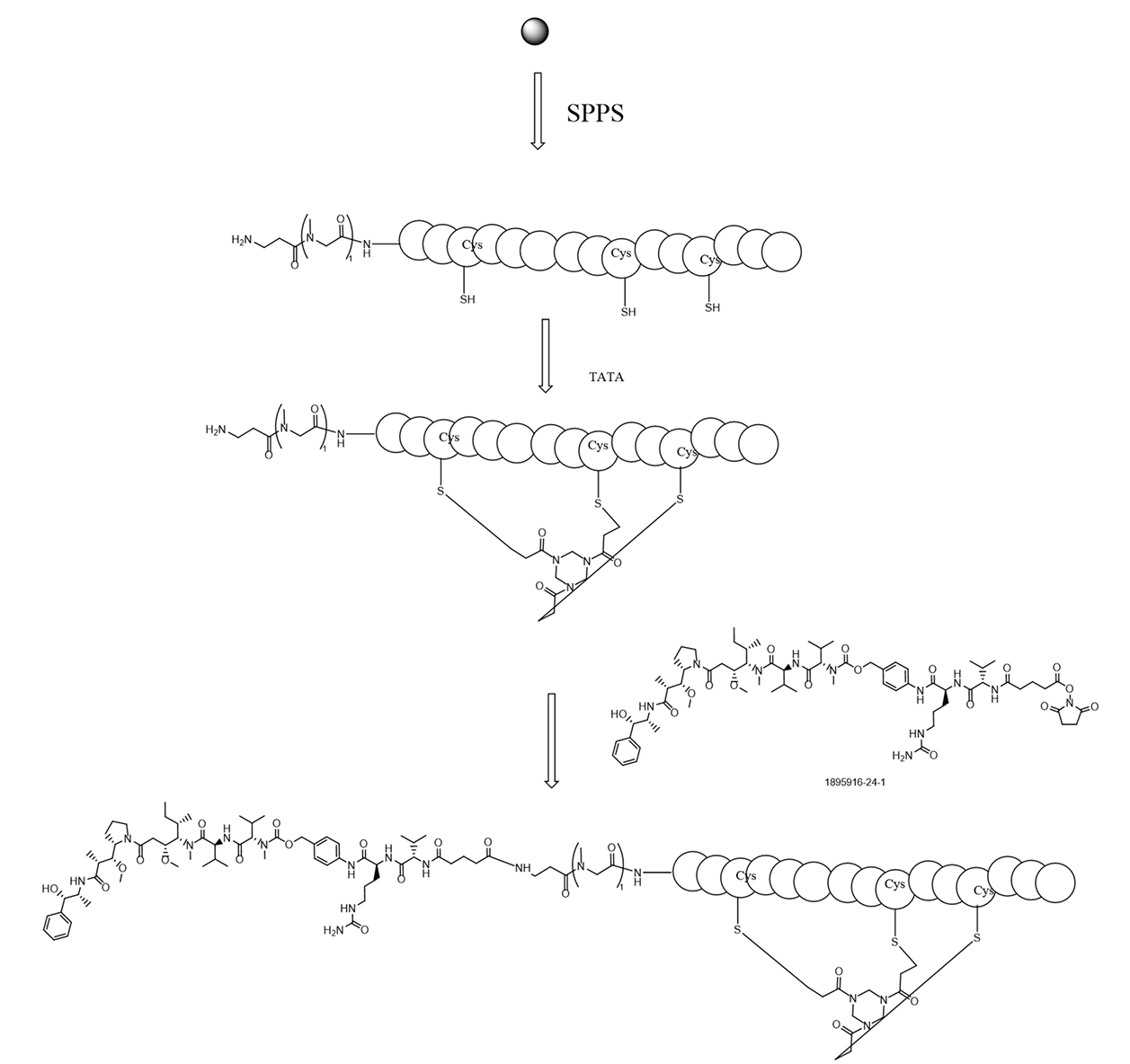
在PDC活性酯偶联中,常规条件下环化和偶联效率不足,难以保证产品纯度。我们通过固相合成和反应条件优化,有效提升了环化和偶联转化率。最终实现了环化收率91%、偶联转化率>85%,并能稳定制备克级PDC,产品纯度超过98%。
常见问题解答
我们的多肽合成平台采用固相与液相合成相结合,具备高通量、自动化生产线,支持快速筛选与合成。我们可合成长度为 3–80 个氨基酸的多肽,并且能够根据需求提供从毫克级到公斤级的合成服务。同时,我们也支持开发环肽(包括多对环结构)、荧光标记等特殊功能化多肽。
我们的生产规模可达克级至公斤级/批次,提供 Non-GMP 和 GMP 双线产能。我们的 GMP 产线配备防爆合成区域,纯化与冻干工艺在 D 级洁净区进行,出料环节可升级至 D-A 区,能够满足多肽原料药级别生产要求。
手性杂质是指在多肽合成过程中,由于消旋反应或其他原因导致的非目标手性异构体。手性杂质可能影响多肽的药效、安全性和稳定性,特别是在临床应用中,可能导致药物活性降低或产生副作用。
多肽手性杂质的控制主要通过以下几种策略实现:
· 起始物料控制:确保所用起始物料具有高纯度,并制定详细的质量标准,避免不合格的起始物料引入杂质。
· 过程控制:在合成过程中,通过筛选合适的反应条件(如温度、溶剂、pH 等),尽量避免消旋反应的发生,减少不必要的手性杂质。
· 工艺控制:采用特殊的工艺策略,如选择手性试剂或酶催化反应等,降低消旋的风险,确保最终产品的手性纯度。
多肽结构的确证是保证产品质量和功能的关键环节。我们采用多种分析手段进行综合确认,包括:核磁共振(¹H-NMR)、质谱(MS)、MS/MS-测序、N-测序、二维核磁(2D-NMR)、红外光谱(IR)以及紫外光谱(UV)。这些方法可从不同维度验证多肽的结构、序列和纯度,确保结果的准确性和可靠性。




